Đối với các bác sĩ chuyên khoa tiêu hóa, việc cập nhật liên tục cơ chế bệnh sinh, chiến lược chẩn đoán sớm và các phác đồ điều trị đa mô thức là vô cùng cấp thiết, bởi chỉ có sự phối hợp nhịp nhàng giữa chẩn đoán hình ảnh, nội soi can thiệp, hóa trị liệu và phẫu thuật mới có thể cải thiện dù chỉ một phần nhỏ tiên lượng của bệnh nhân.
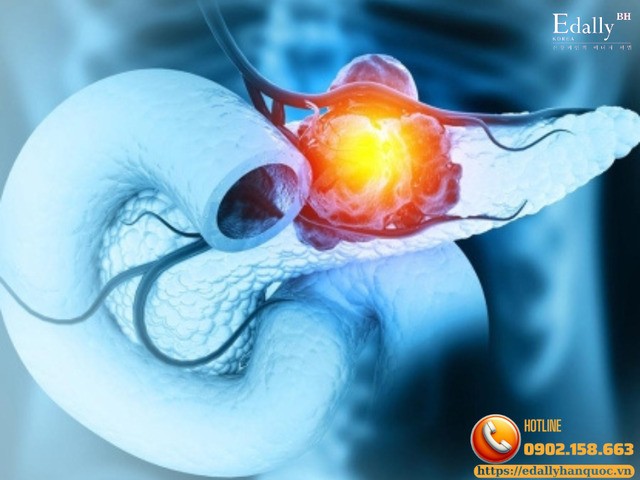
Mặc dù nguyên nhân chính xác gây ung thư tụy vẫn chưa được xác định hoàn toàn, đa số trường hợp xảy ra lẻ tẻ không có tiền sử gia đình. Tuy nhiên, các yếu tố nguy cơ được chứng minh qua nhiều nghiên cứu dịch tễ học lớn bao gồm:
Hút thuốc lá: là yếu tố nguy cơ quan trọng nhất có thể thay đổi được, làm tăng nguy cơ từ 2 đến 3 lần. Nicotine và các nitrosamine đặc hiệu thuốc lá gây tổn thương DNA tế bào tụy ngoại tiết.
Uống rượu mạn tính: liên quan rõ ràng với viêm tụy mạn, sau đó tăng nguy cơ ung thư tụy (gấp 2-3 lần nếu viêm tụy mạn do rượu). Tuy nhiên, bản thân rượu nếu không gây viêm tụy thì nguy cơ tăng không đáng kể.
Béo phì và lối sống ít vận động: béo phì (BMI >30) làm tăng nguy cơ khoảng 20-50%. Mô mỡ nội tạng thúc đẩy kháng insulin, viêm mạn và tăng các yếu tố tăng trưởng như IGF-1.
Chế độ ăn: chế độ ăn giàu thịt đỏ, thịt chế biến sẵn, chất béo bão hòa có thể làm tăng nguy cơ, trong khi chế độ ăn nhiều rau củ quả, axit folic có vai trò bảo vệ.
Viêm tụy mạn: đặc biệt viêm tụy mạn di truyền (đột biến gen PRSS1, SPINK1, CFTR) có nguy cơ ung thư hóa rất cao, ước tính 30-40% ở tuổi 70. Viêm tụy mạn thể vô căn cũng làm tăng nguy cơ gấp 10-20 lần.
Đái tháo đường: đái tháo đường type 2 mới khởi phát (dưới 3 năm) có thể vừa là yếu tố nguy cơ vừa là hậu quả sớm của ung thư tụy. Ngược lại, đái tháo đường type 1 kéo dài >10 năm cũng tăng nguy cơ nhẹ.
Nang tụy: đặc biệt nang nhầy có ống tụy (IPMN) nhánh chính và nang nhầy (MCN) có nguy cơ thoái hóa ác tính cao cần được theo dõi và cắt khi có dấu hiệu bất thường.
Khoảng 5-10% ung thư tụy có tính chất gia đình. Các hội chứng di truyền làm tăng nguy cơ đáng kể:
Hội chứng Peutz-Jeghers (đột biến STK11): nguy cơ ung thư tụy suốt đời lên tới 30-40%.
Hội chứng ung thư vú - buồng trứng di truyền (BRCA1, BRCA2): đột biến BRCA2 làm tăng nguy cơ gấp 3-10 lần.
Hội chứng Lynch (HNPCC): đột biến gen sửa sai MLH1, MSH2, MSH6.
Viêm tụy di truyền (PRSS1). Hội chứng FAMMM (melanoma đa dạng gia đình, đột biến CDKN2A/p16).
Hội chứng Li-Fraumeni (TP53), hội chứng FAP (APC).
Tuổi: cực kỳ hiếm dưới 40 tuổi; đỉnh cao 65-75 tuổi.
Giới: nam cao hơn nữ nhẹ (tỷ lệ khoảng 1,3:1).
Nhóm máu: người nhóm máu non-O (A, B, AB) có nguy cơ cao hơn nhóm O, cơ chế liên quan đến kháng nguyên Lewis và viêm mạn.
Nhiễm H.pylori và virus viêm gan B: một số nghiên cứu gợi ý nhưng chưa kết luận chắc chắn.
Sinh bệnh học ung thư tụy đã được làm sáng tỏ đáng kể nhờ các công nghệ giải trình tự gen thế hệ mới. Bệnh được hình thành qua quá trình nhiều bước, từ tổn thương tiền ung thư (PanIN, IPMN, MCN) đến ung thư xâm lấn, tích lũy dần các đột biến gen đặc trưng.
KRAS: đột biến điểm (thường codon 12) xuất hiện rất sớm, gần như 100% ung thư biểu mô ống tụy có đột biến này. KRAS hoạt hóa liên tục các con đường tín hiệu MAPK, PI3K-AKT, RAL, thúc đẩy tăng sinh, sống sót và chuyển dạng.
CDKN2A/p16: mất chức năng (đột biến, mất đoạn đồng hợp tử, methyl hóa vùng khởi động) xảy ra ở giai đoạn PanIN-2/PanIN-3, mất kiểm soát chu kỳ tế bào tại điểm kiểm tra G1/S, cho phép tế bào nhân lên bất thường.
TP53: đột biến mất chức năng ở giai đoạn muộn (PanIN-3 trở đi), mất cơ chế apoptosis và sửa sai DNA, tạo điều kiện cho tế bào khối u tồn tại dưới áp lực thiếu oxy và tổn thương DNA.
SMAD4/DPC4: đột biến hoặc mất đoạn đồng hợp tử gặp trong 50-60% trường hợp, liên quan đến di căn xa và tiên lượng xấu. SMAD4 là thành phần quan trọng của con đường TGF-β (ức chế tăng trưởng và cảm ứng apoptosis).
Các đột biến khác: ARID1A, KDM6A, RNF43, GNAS (đặc biệt trong IPMN), BRAF (hiếm, đáp ứng với thuốc ức chế BRAF).
Mất đoạn lớn nhiễm sắc thể (ví dụ 9p21, 17p13, 18q21). Các chuyển đoạn, khuếch đại (MYC, AKT2, KRAS khuếch đại ở di căn).
Mất ổn định vi vệ tinh (MSI) gặp dưới 1% ung thư tụy thông thường, nhưng phổ biến hơn ở thể liên quan hội chứng Lynch (khoảng 3-4%), có ý nghĩa với điều trị bằng ức chế điểm kiểm soát miễn dịch.
Ung thư tụy nổi tiếng với mô đệm xơ hóa dày đặc (desmoplasia), chiếm tới 80% thể tích khối u. Thành phần mô đệm bao gồm:
Nguyên bào sợi liên quan ung thư (CAFs): tiết các cytokine, chemokine (IL-6, CXCL12, TGF-β, HGF), collagen, acid hyaluronic, tạo áp lực kẽ cao, ngăn cản tưới máu và thấm thuốc.
Tế bào miễn dịch ức chế: đại thực bào M2 (dòng TAM), tế bào T điều hòa (Treg), tế bào supressor có nguồn gốc myeloid (MDSC). Chúng tạo ra môi trường ức chế miễn dịch, giúp khối u trốn tránh sự tấn công của hệ thống miễn dịch và kháng liệu pháp miễn dịch.
Chất nền ngoại bào dày đặc: hyaluronan, collagen, fibronectin, làm khối u cứng, gây thiếu oxy mạn tính, kích thích tế bào ung thư chuyển sang cơ chế trao đổi chất hiếu khí (glycolysis kỵ khí) - hiệu ứng Warburg.
Sự tương tác giữa tế bào ung thư và mô đệm tạo thành một vòng luẩn quẩn thúc đẩy xâm lấn, di căn và kháng trị.
Ung thư tụy được mệnh danh là "kẻ giết người thầm lặng" bởi giai đoạn đầu hầu như không có triệu chứng hoặc triệu chứng rất mơ hồ. Khi xuất hiện triệu chứng rõ rệt, phần lớn bệnh đã ở giai đoạn tiến triển không còn khả năng phẫu thuật triệt căn.
Vàng da tắc mật: là triệu chứng sớm nhất thường gặp khi u ở đầu tụy. Vàng da (do bilirubin trực tiếp tăng) có thể khởi phát âm thầm hoặc đột ngột, kèm theo ngứa da, phân bạc màu, nước tiểu sẫm màu. Khác với sỏi mật, vàng da trong ung thư tụy thường tiến triển tăng dần, không đau, đôi khi kèm túi mật to chạm được (dấu hiệu Courvoisier - Terrier: túi mật căng to, không đau trong bệnh lý ác tính vùng bóng Vater).
Đau bụng: đau vùng thượng vị hoặc hạ sườn phải (nếu u đầu tụy) hoặc đau lan ra sau lưng (u thân - đuôi tụy xâm lấn đám rối thần kinh tạng). Đau thường âm ỉ, liên tục, tăng khi nằm ngửa và giảm khi ngồi cúi về phía trước. Đau dữ dội, thường xuyên gợi ý xâm lấn sau phúc mạc hoặc di căn xương.
Hội chứng tắc nghẽn dạ dày - tá tràng: khi u xâm lấn hoặc chèn ép đoạn D2-D3 tá tràng, gây buồn nôn, nôn sau ăn, bụng chướng.
Sút cân nhanh: gần như tất cả bệnh nhân đều sụt cân, trung bình 5-10 kg trong vài tháng. Nguyên nhân do chán ăn, kém hấp thu (thiếu men tụy), tiêu hao năng lượng do khối u và các cytokine viêm (cachectin/TNF-α).
Suy nhược, mệt mỏi, đôi khi sốt nhẹ kéo dài không rõ nguyên nhân.
Đái tháo đường mới khởi phát hoặc đái tháo đường trước đó trở nên nặng hơn, khó kiểm soát. Đây có thể là dấu hiệu báo động sớm cần được tầm soát ung thư tụy, đặc biệt ở người trên 50 tuổi không béo phì, không yếu tố gia đình.
Di căn gan: gan to, đau hạ sườn phải, cổ trướng, tăng men gan, rối loạn đông máu.
Di căn phúc mạc: cổ trướng ác tính, rối loạn nhu động ruột.
Di căn xương: đau xương (thường cột sống, xương chậu, xương sườn), gãy xương bệnh lý.
Di căn não, phổi, màng phổi ít gặp hơn.
Túi mật to (dấu hiệu Courvoisier) gặp trong khoảng 25-40% u đầu tụy.
Khối u sờ thấy ở vùng thượng vị hoặc hạ sườn trái (thường gặp khi u thân - đuôi tụy kích thước lớn).
Cổ trướng, lách to (di căn hoặc huyết khối tĩnh mạch lách/tĩnh mạch cửa).
Hạch thượng đòn trái (hạch Virchow) hoặc hạch rốn (hạch Sister Mary Joseph) gợi ý di căn xa.
Dấu hiệu Trousseau: viêm tĩnh mạch huyết khối di chuyển ở các chi, thường gặp trong ung thư tụy (hội chứng cận ung thư, do giải phóng mucin và yếu tố đông máu).
Lưu ý quan trọng cho bác sĩ: nhiều bệnh nhân được chẩn đoán ở giai đoạn sớm nhờ tình cờ phát hiện vàng da hoặc bất thường men tụy. Không có triệu chứng nào đủ nhạy hoặc đặc hiệu để chẩn đoán sớm; do đó cần có chỉ định chụp cắt lớp vi tính (CLVT) thấp ngưỡng ở nhóm nguy cơ cao.
Chẩn đoán ung thư tụy dựa trên phương tiện hình ảnh học và sinh thiết (mô bệnh học hoặc tế bào học) kết hợp với dấu ấn khối u. Mục tiêu chính: xác định bản chất ung thư, đánh giá khả năng cắt bỏ (resectability) và phân loại giai đoạn TNM.
Cắt lớp vi tính (CLVT) đa dãy đầu dò: là tiêu chuẩn vàng để chẩn đoán, phân loại giai đoạn và lập kế hoạch phẫu thuật. Kỹ thuật: tiêm thuốc cản quang tĩnh mạch, thì tụy (40-50 giây) và thì cửa (70-80 giây). Đánh giá khối u, liên quan với động mạch thân tạng, động mạch mạc treo tràng trên, tĩnh mạch cửa, tĩnh mạch mạc treo tràng trên. Tiêu chí không cắt bỏ được bao gồm: xâm lấn động mạch >180°, bít tắc tĩnh mạch cửa không thể tái tạo, di căn gan hoặc phúc mạc.
Cộng hưởng từ (MRI) và mật tụy cộng hưởng từ (MRCP): có giá trị tương đương với CLVT, đặc biệt đối với bệnh nhân suy thận hoặc dị ứng thuốc cản quang iod. MRI có ưu thế hơn trong đánh giá tổn thương nang và u tế bào đảo tụy.
Siêu âm nội soi (EUS): có độ phân giải cao, phát hiện khối u nhỏ <2 cm, cho phép sinh thiết kim nhỏ (EUS-FNA/ FNB) để lấy mô bệnh học. Độ nhạy và độ đặc hiệu trên 85-90%. EUS cũng đánh giá xâm lấn mạch máu và hạch vùng. Lưu ý: EUS-FNB (sinh thiết lõi) đang thay thế FNA vì lấy được nhiều mô hơn.
Chụp cắt lớp phát xạ positron (PET/CT) với FDG: chỉ định trong trường hợp nghi ngờ di căn không xác định, hoặc theo dõi tái phát. PET/CT độ nhạy cao với tổn thương >1 cm, nhưng dương tính giả trong viêm tụy cấp/mạn. Không dùng thường quy để chẩn đoán ban đầu.
Chụp mật tụy ngược dòng (ERCP): ngày nay ít dùng để chẩn đoán, chủ yếu để can thiệp (đặt stent mật trong tắc nghẽn, lấy mảnh ghép tế bào - chải bàn chải, sinh thiết qua soi. Tuy nhiên sinh thiết qua ERCP có độ nhạy thấp hơn EUS-FNA.
Chỉ định sinh thiết bắt buộc trước khi điều trị hóa/xạ trị tân bổ trợ hoặc giảm nhẹ. Trường hợp có thể phẫu thuật triệt căn ngay, có thể phẫu thuật không cần sinh thiết trước (phẫu thuật cũng là chẩn đoán).
EUS-FNA/FNB là phương pháp được ưu tiên hàng đầu. Độ an toàn cao (tỷ lệ biến chứng viêm tụy cấp khoảng 0,5%, xuất huyết <1%).
Sinh thiết qua da dưới hướng dẫn CLVT hoặc siêu âm: khi không thể EUS (ví dụ u đuôi tụy lớn, hoặc chống chỉ định nội soi). Nguy cơ gieo rắc tế bào theo đường kim khoảng 1-2% nhưng thường chấp nhận được nếu không có lựa chọn khác.
CA 19-9 (carbohydrate antigen 19-9): là dấu ấn hữu ích nhất. Tăng trong 70-80% ung thư tụy giai đoạn tiến triển. Giá trị cắt thường dùng 37 U/mL. Tuy nhiên, CA 19-9 không nhạy trong giai đoạn sớm, có thể dương tính giả trong viêm đường mật, viêm tụy, xơ gan, tắc mật. Đặc biệt người nhóm máu Lewis (a-b-) không tiết kháng nguyên, CA 19-9 sẽ âm tính giả. Sử dụng CA 19-9 để theo dõi đáp ứng điều trị và phát hiện tái phát sau mổ, hơn là chẩn đoán ban đầu.
CEA (carcinoembryonic antigen): ít đặc hiệu, thường tăng nhẹ, có giá trị hỗ trợ.
Các dấu ấn mới như CA 125, TFPI2, thrombospondin-2, miRNA đang được nghiên cứu nhưng chưa đưa vào thực hành lâm sàng.
Giai đoạn TNM đối với ung thư biểu mô ống tụy:
T: Tis (carcinoma in situ), T1 (≤2 cm), T2 (>2-4 cm), T3 (>4 cm hoặc xâm lấn ngoài tụy), T4 (xâm lấn động mạch thân tạng, mạc treo tràng trên hoặc gốc động mạch gan chung)
N: N0 (không hạch), N1 (1-3 hạch), N2 (≥4 hạch)
M: M0 (không di căn), M1 (di căn xa)
Nhóm giai đoạn lâm sàng:
Giai đoạn IA: T1 N0 M0
Giai đoạn IB: T2 N0 M0
Giai đoạn IIA: T3 N0 M0
Giai đoạn IIB: T1-3 N1 M0
Giai đoạn III: T4 bất kỳ N M0 hoặc bất kỳ T N2 M0
Giai đoạn IV: bất kỳ T bất kỳ N M1
Phân loại khả năng cắt bỏ (quan trọng cho quyết định điều trị):
Cắt bỏ được (Resectable): u không tiếp xúc mạch máu động mạch (>180° vòng cung không tiếp xúc), tĩnh mạch cửa hoặc tĩnh mạch mạc treo tràng trên không tiếp xúc hoặc tiếp xúc ≤180° nhưng không có biến dạng.
Cắt bỏ ranh giới (Borderline resectable): tiếp xúc động mạch ≤180°, hoặc tiếp xúc tĩnh mạch >180° nhưng có thể tái tạo, hoặc tiếp xúc động mạch gan chung nhưng chưa tới gốc. Những trường hợp này cần hóa/xạ trị tân bổ trợ trước mổ.
Không cắt bỏ được - tại chỗ tiến triển (Locally advanced): xâm lấn động mạch >180° hoặc bít tắc tĩnh mạch cửa/ mạc treo tràng trên không thể tái tạo, nhưng chưa di căn xa.
Di căn xa (Metastatic).
Dưới đây là hệ thống phân loại toàn diện theo góc nhìn của chuyên gia nội ung thư - giải phẫu bệnh.
Ung thư biểu mô ống tụy (Pancreatic ductal adenocarcinoma - PDAC): chiếm >90% các trường hợp. Biểu hiện các tuyến, ống không đều, mô đệm xơ hóa dày. Các biến thể: thể tuyến vảy, thể sarcomatoid, thể tế bào sáng, thể tế bào nhẫn, thể không biệt hóa - đều có tiên lượng xấu hơn thể thông thường.
U nang nhầy (Mucinous cystic neoplasm with invasive carcinoma): hiếm, liên quan vùng thân đuôi, gặp ở phụ nữ.
IPMN (Intraductal papillary mucinous neoplasm) với xâm lấn: liên quan đến lòng ống chính hoặc nhánh, tiết dịch nhầy.
Các loại ít gặp: ung thư tế bào acinar, ung thư tụy thể u nang (solid-pseudopapillary neoplasm), u thần kinh nội tiết, u nguyên bào tụy.
Phân loại Collisson (2011): 3 subtype dựa trên dữ liệu biểu hiện gen: cổ điển (classical - biểu hiện gen biểu mô và chuyển hóa lipid, tiên lượng tốt hơn), nguyên bào mô đệm (quasi-mesenchymal - biểu hiện gen trung mô, xâm lấn cao), ngoại tiết (exocrine-like). Subtype cổ điển nhạy với gemcitabine hơn.
Phân loại Bailey (2016): 4 subtype: squamous (liên quan sừng hóa, p63, TP63, đáp ứng kém), pancreatic progenitor (biểu hiện PDX1, FOXA2, khá hơn), immunogenic (tăng thâm nhiễm tế bào miễn dịch, có tiềm năng đáp ứng liệu pháp miễn dịch), aberrantly differentiated endocrine exocrine (ADEX). Việc phân loại phân tử đang từng bước được ứng dụng để lựa chọn liệu pháp nhắm trúng đích và thử nghiệm lâm sàng.
Điều trị ung thư tụy đòi hỏi chiến lược đa mô thức, bao gồm phẫu thuật, hóa trị, xạ trị và chăm sóc giảm nhẹ. Lựa chọn phụ thuộc vào giai đoạn bệnh khi chẩn đoán, tình trạng toàn thân bệnh nhân (ECOG PS), tuổi, bệnh lý kèm và sở thích của người bệnh.
Là phương pháp duy nhất mang lại cơ hội chữa khỏi, nhưng chỉ được thực hiện ở dưới 20% bệnh nhân khi chẩn đoán.
Các phẫu thuật :
Phẫu thuật Whipple (pancreaticoduodenectomy - PD): dành cho u đầu tụy. Cắt bỏ đầu tụy, tá tràng, đoạn xa ống mật chủ, túi mật, mỏm vị - tái lập lưu thông bằng nối tụy - hỗng tràng, mật - hỗng tràng, dạ dày - hỗng tràng. Tỷ lệ tử vong tại các trung tâm lớn <3-5%, biến chứng rò tụy khoảng 10-20%.
PD bảo tồn môn vị (Pylorus-preserving PD): có lợi ích dinh dưỡng và dạ dày tốt hơn, không khác biệt về sống còn.
Phẫu thuật cắt đuôi tụy + lách (Distal pancreatectomy + splenectomy): dành cho u thân - đuôi tụy. Có thể nội soi ở các trung tâm có kinh nghiệm.
Cắt toàn bộ tụy: hiếm khi chỉ định do hậu quả nặng nề (đái tháo đường, suy tiêu hóa ngoại tiết), chỉ khi u lan tỏa toàn bộ tụy hoặc đa ổ.
Phẫu thuật cắt bỏ mạch máu: trong trường hợp xâm lấn tĩnh mạch cửa - tĩnh mạch mạc treo tràng trên nhưng còn khả năng cắt và nối, có thể được thực hiện tại các trung tâm có nhiều kinh nghiệm, không làm xấu tiên lượng nếu được cắt bỏ hoàn toàn (R0).
Vai trò của hóa trị tân bổ trợ và bổ trợ:
Hóa trị bổ trợ (adjuvant) sau phẫu thuật bắt buộc cho tất cả bệnh nhân đã phẫu thuật triệt căn, trừ khi quá yếu. Phác đồ chuẩn: mFOLFIRINOX (giảm liều 5-FU so với dùng trong di căn) hoặc gemcitabine + capecitabine hoặc gemcitabine đơn thuần (cho người già hoặc PS kém). Nghiên cứu PRODIGE 24 cho thấy mFOLFIRINOX cải thiện sống còn trung bình lên 54,4 tháng so với gemcitabine 35 tháng.
Hóa trị tân bổ trợ (neoadjuvant) được chỉ định cho ung thư tụy ranh giới cắt bỏ hoặc tại chỗ tiến triển. Mục tiêu giảm kích thước khối u, tăng tỷ lệ cắt bỏ R0, loại bỏ vi di căn. Phác đồ thường dùng: FOLFIRINOX +/- xạ trị đồng thời hoặc gemcitabine + nab-paclitaxel.
Thể trạng tốt (PS 0-1): FOLFIRINOX (oxaliplatin, irinotecan, leucovorin, 5-FU) đã làm thay đổi lịch sử điều trị, đạt đáp ứng 31,6%, sống còn trung bình 11,1 tháng. Tuy nhiên độc tính cao. Hoặc gemcitabine + nab-paclitaxel (cải thiện sống còn 8,5 tháng so với gemcitabine 6,7 tháng). Lựa chọn giữa 2 phác đồ dựa trên độc tính dự kiến và sở thích bệnh nhân.
Thể trạng trung bình (PS 2): gemcitabine đơn thuần, hoặc gemcitabine + capecitabine (tác dụng phụ nhẹ hơn), hoặc 5-FU + oxaliplatin (FOLFOX).
Thể trạng yếu (PS ≥3): chăm sóc giảm nhẹ tối ưu, không hóa trị.
Đột biến BRCA1/2: nhạy với platinum (oxaliplatin, cisplatin) và đặc biệt với ức chế PARP (olaparib) trong điều trị duy trì cho bệnh di căn ổn định sau platinum. Đây là liệu pháp nhắm trúng đích đầu tiên được chấp thuận cho ung thư tụy (FDA 2019).
MSI cao (dưới 1%): miễn dịch trị liệu pembrolizumab (ức chế PD-1) có đáp ứng cao và bền vững.
Các đột biến khác (NTRK, BRAF, HER2, KRAS G12C): đã có các thuốc ức chế tương ứng, nhưng tỷ lệ thấp, chỉ thử nghiệm hoặc ngoài nhãn.
Vai trò còn nhiều tranh cãi, nhưng có thể sử dụng:
Xạ trị tiền phẫu (neoadjuvant) trong u ranh giới cắt bỏ hoặc u tại chỗ tiến triển kết hợp với hóa trị liệu (thường là capecitabine hoặc 5-FU). Kỹ thuật xạ có thể IMRT hay SBRT (liều cao vài phân liều).
Xạ trị giảm nhẹ đau sau phúc mạc khi đau kháng trị.
Không khuyến cáo xạ trị bổ trợ thường quy sau phẫu thuật triệt căn vì các thử nghiệm không cho thấy lợi ích sống còn.
Dẫn lưu mật qua da hoặc nội soi (ERCP đặt stent kim loại tự nở) cho bệnh nhân vàng da tắc mật không thể phẫu thuật.
Điều trị đau: opioids (morphine, fentanyl, oxycodone). Khi đau nhiều do xâm lấn đám rối thần kinh tạng, có thể phong bế thần kinh tạng qua EUS hoặc qua da bằng ethanol. Giảm đau bằng xạ trị cũng có hiệu quả.
Suy dinh dưỡng và suy tụy ngoại tiết: thay thế men tụy (pancreatin) mỗi bữa ăn (25.000-50.000 đơn vị lipase), hỗ trợ dinh dưỡng, tư vấn chế độ ăn giàu năng lượng, protein, NK bổ sung đường uống.
Huyết khối tĩnh mạch: dự phòng bằng heparin trọng lượng phân tử thấp (LMWH) ở bệnh nhân nằm viện hoặc bất động; điều trị kháng đông nếu có huyết khối.
Cổ trướng ác tính: chọc dò, lợi tiểu (spironolactone, furosemide), đặt dẫn lưu bụng ra ngoài lâu dài khi kháng trị.
Hỗ trợ tâm lý và chăm sóc cuối đời: cần thiết từ sớm.
Một điểm mới: các thử nghiệm lâm sàng đang tích cực đánh giá liệu pháp ức chế điểm kiểm soát (anti-PD-1, anti-CTLA-4, anti-LAG-3), vaccine, liệu pháp tế bào CAR-T, ức chế KRAS đặc hiệu (như MRTX1133 cho KRAS G12D, sotorasib/adagrasib cho G12C), ức chế mô đệm (PEGPH20 – hyaluronidase, ức chế FAK, ức chế CXCR4). Hy vọng sớm có thêm lựa chọn.
Biến chứng của ung thư tụy có thể do khối u gây ra hoặc do điều trị.
Tắc mật ác tính: dẫn đến nhiễm trùng đường mật, suy gan, rối loạn đông máu.
Tắc tá tràng: gây hẹp môn vị, nôn, không thể ăn uống, cần nối vị tránh hoặc đặt stent tiêu hóa.
Chảy máu đường tiêu hóa: do xâm lấn tá tràng hoặc dạ dày, hoặc vỡ giả phình mạch vùng.
Huyết khối tĩnh mạch sâu và thuyên tắc phổi (hội chứng Trousseau).
Đái tháo đường và suy tụy ngoại tiết nặng.
Cổ trướng ác tính, gan to, suy kiệt, nhiễm trùng cơ hội.
Phẫu thuật: rò tụy (phổ biến nhất, xử trí bằng dẫn lưu, somatostatin, dinh dưỡng), chậm làm rỗng dạ dày, chảy máu, áp xe ổ bụng, nhiễm trùng vết mổ, suy tụy nội/ngoại tiết sau mổ.
Hóa trị: độc tính tủy xương (giảm bạch cầu, thiếu máu, giảm tiểu cầu), buồn nôn nôn, viêm niêm mạc, tiêu chảy (irinotecan), bệnh lý thần kinh ngoại biên (oxaliplatin), rụng tóc, mệt mỏi, độc tính tim (5-FU hiếm).
Xạ trị: viêm da, mệt mỏi, buồn nôn, viêm dạ dày - tá tràng, hẹp tá tràng muộn.
Can thiệp nội soi mật: viêm tụy cấp sau ERCP (3-5%), thủng tá tràng, chảy máu, viêm đường mật, tắc stent.
Tiên lượng sống ở bệnh nhân ung thư tụy vẫn còn rất nặng nề so với hầu hết các ung thư khác.
Tỷ lệ sống còn toàn bộ: Tỷ lệ sống sau 5 năm tổng thể ở mọi giai đoạn chỉ khoảng 10-12% (SEER 2010-2019). Tỷ lệ này có cải thiện nhẹ so với 5-6% của thập niên 2000, nhưng vẫn thấp.
Theo giai đoạn: Nếu được phát hiện ở giai đoạn khu trú (localized – gần 15% bệnh nhân), sống còn 5 năm khoảng 42-44% sau phẫu thuật triệt căn + hóa trị bổ trợ. Giai đoạn tại chỗ tiến triển còn dưới 12%. Di căn xa thì hầu như không khỏi, sống còn trung bình 6-12 tháng dù điều trị tích cực.
Các yếu tố tiên lượng tốt hơn: cắt bỏ hoàn toàn R0, không di căn hạch, kích thước u nhỏ, độ mô học thấp, CA 19-9 bình thường hóa sau mổ, thể cổ điển phân tử, đột biến BRCA/ MSI (dù ít gặp), thể trạng tốt, không có triệu chứng suy kiệt.
Yếu tố tiên lượng xấu: CA 19-9 cao, mất SMAD4, đột biến TP53, xâm lấn mạch máu, hạch nhiều (>3), tái phát sớm sau mổ (<6-12 tháng), điểm ECOG ≥2, có cổ trướng.
Điều đáng chú ý: ngay cả sau phẫu thuật triệt căn, tỷ lệ tái phát trong vòng 2 năm lên tới 70-80%, thường tại gan, phúc mạc, hoặc bờ nối tụy. Điều này nhấn mạnh nhu cầu cấp thiết về các liệu pháp toàn thân hiệu quả hơn và chiến lược tầm soát quần thể nguy cơ cao.
Chẩn đoán sớm còn nan giải: không có phương pháp sàng lọc đại trà cho dân số chung. Với nhóm nguy cơ rất cao (viêm tụy di truyền, hội chứng Peutz-Jeghers, đột biến BRCA2, CDKN2A gia đình), có thể siêu âm nội soi hoặc cộng hưởng từ hàng năm bắt đầu từ tuổi 50 hoặc sớm hơn 10 năm so với tuổi mắc bệnh sớm nhất trong gia đình.
Mới phát hiện đái tháo đường >50 tuổi, sút cân: nên nghĩ tới ung thư tụy và làm CA 19-9, CLVT ổ bụng nếu không tìm thấy nguyên nhân rõ ràng sau 6 tháng.
Xử trí thận trọng với nang tụy: nang IPMN nhánh chính ≥10 mm, có nhân vách, đường kính ống tụy chính ≥10 mm, hoặc thay đổi kích thước nhanh >3 mm/năm là chỉ định cắt tụy. EUS-FNA khi nghi ngờ cao.
Tối ưu hóa liệu pháp tân bổ trợ: với u ranh giới cắt bỏ, không vội vàng mổ. Hội chẩn liên chuyên khoa (Hội đồng ung thư tụy) để quyết định hóa trị trước mổ.
Quản lý độc tính hóa trị: đặc biệt với FOLFIRINOX cần giảm liều irinotecan, 5-FU ở người trên 75 tuổi, suy thận, suy gan nhẹ; dự phòng sốt giảm bạch cầu bằng G-CSF.
Sử dụng xét nghiệm giải trình tự gen khối u (NGS) cho bệnh nhân di căn để phát hiện đột biến hiếm (BRCA, MSI, NTRK, ROS1, BRAF...) có thuốc nhắm đích.
Điều trị giảm nhẹ chủ động: đừng chỉ tập trung vào hóa trị. Giảm đau, dinh dưỡng, men tụy, dẫn lưu mật, chăm sóc tâm lý xã hội cần song hành ngay từ đầu.
Tham khảo các sản phẩm chăm sóc sức khỏe chính hãng tại: https://edallyhanquoc.vn/thuc-pham-bao-ve-suc-khoe-edally-bh-han-quoc.html
Mọi thông tin chi tiết về sản phẩm cũng như chính sách đại lý xin vui lòng liên hệ edallyhanquoc.vn qua Hotline/Zalo: 0902.158.663 để được tư vấn và hỗ trợ nhanh nhất.
Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer Statistics, 2022. CA Cancer J Clin. 2022;72(1):7-33.
Mizrahi JD, Surana R, Valle JW, Shroff RT. Pancreatic cancer. Lancet. 2020;395(10242):2008-2020.
Ryan DP, Hong TS, Bardeesy N. Pancreatic adenocarcinoma. N Engl J Med. 2014;371(22):2140-2141.
Conroy T, Hammel P, Hebbar M, et al. FOLFIRINOX or gemcitabine as adjuvant therapy for pancreatic cancer. N Engl J Med. 2018;379(25):2395-2406.
Von Hoff DD, Ervin T, Arena FP, et al. Increased survival in pancreatic cancer with nab-paclitaxel plus gemcitabine. N Engl J Med. 2013;369(18):1691-1703.
Tempero MA, Malafa MP, Al-Hawary M, et al. Pancreatic Adenocarcinoma, Version 2.2021, NCCN Cl
 Suy Giáp: Bệnh Dễ Bị Bỏ Sót Nhưng Hoàn Toàn Có Thể Kiểm Soát Tốt
Suy Giáp: Bệnh Dễ Bị Bỏ Sót Nhưng Hoàn Toàn Có Thể Kiểm Soát Tốt
 Chóng Mặt Tư Thế Kịch Phát Lành Tính (BPPV) - Cập Nhật Mới Nhất Từ Jama 2026
Chóng Mặt Tư Thế Kịch Phát Lành Tính (BPPV) - Cập Nhật Mới Nhất Từ Jama 2026
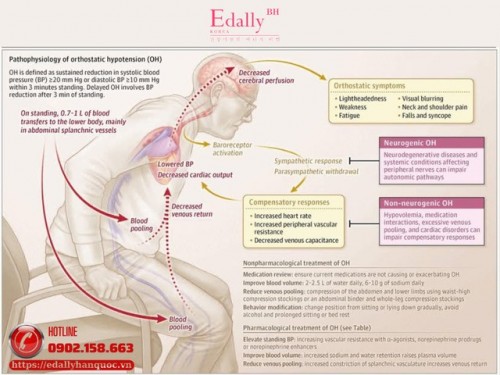 Hạ Huyết Áp Tư Thế - Cập Nhật Mới Nhất Từ Jama 2026
Hạ Huyết Áp Tư Thế - Cập Nhật Mới Nhất Từ Jama 2026
 Huyết Áp Cao Kiểm Soát Kém - Con Đường Ngắn Nhất Dẫn Đến Đột Quỵ
Huyết Áp Cao Kiểm Soát Kém - Con Đường Ngắn Nhất Dẫn Đến Đột Quỵ
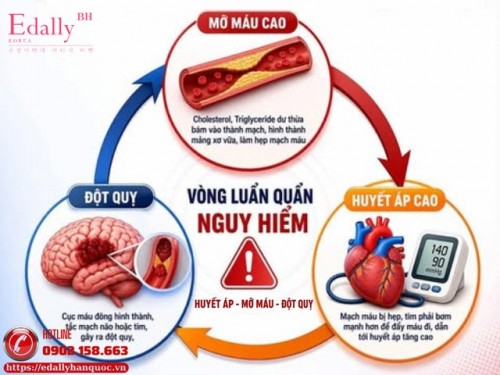 Huyết Áp - Mỡ Máu - Đột Quỵ: Vòng Luẩn Quẩn Nguy Hiểm
Huyết Áp - Mỡ Máu - Đột Quỵ: Vòng Luẩn Quẩn Nguy Hiểm
 Vì Sao Người Bệnh Tiểu Đường Càng Cần Bổ Sung Omega-3 Thường Xuyên?
Vì Sao Người Bệnh Tiểu Đường Càng Cần Bổ Sung Omega-3 Thường Xuyên?
 Hệ thống Theo Dõi Đường Huyết Liên Tục (CGM) - Những Điều Người Bệnh Đái Tháo Đường Cần Biết
Hệ thống Theo Dõi Đường Huyết Liên Tục (CGM) - Những Điều Người Bệnh Đái Tháo Đường Cần Biết
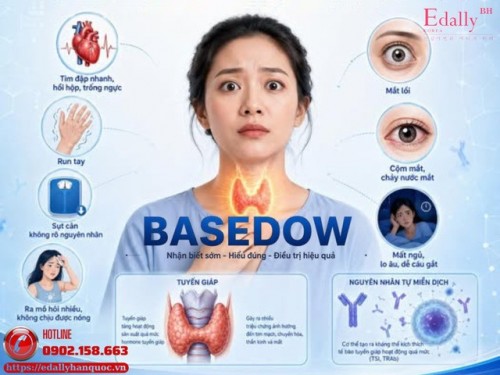 12 Điều Nên Nhớ Để Hiểu Đúng Về Bệnh Basedow
12 Điều Nên Nhớ Để Hiểu Đúng Về Bệnh Basedow
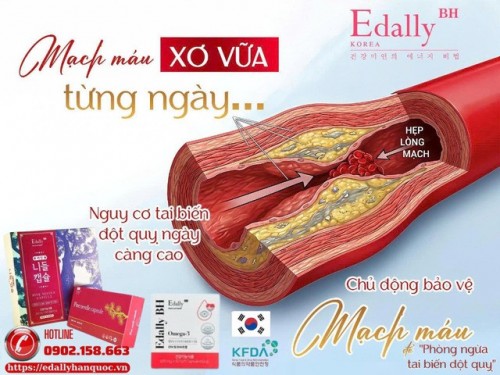 Xơ Vữa Mạch Máu Liên Quan Gì Đến Đột Quỵ?
Xơ Vữa Mạch Máu Liên Quan Gì Đến Đột Quỵ?
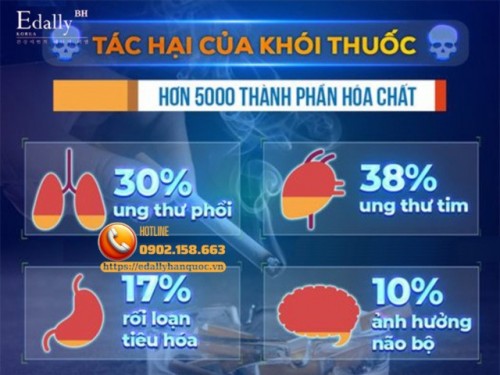 Hút Thuốc Ảnh Hưởng Thế Nào Đến Nguy Cơ Đột Quỵ?
Hút Thuốc Ảnh Hưởng Thế Nào Đến Nguy Cơ Đột Quỵ?
Chia sẻ bài viết:
 Làm Thế Nào Để Hồi Sinh Làn Da Lão Hóa?
Làm Thế Nào Để Hồi Sinh Làn Da Lão Hóa?
 Tại Sao Phải Trẻ Hóa Màng Đáy Trong Điều Trị Nám?
Tại Sao Phải Trẻ Hóa Màng Đáy Trong Điều Trị Nám?
 Lợi Khuẩn Và Vai Trò Đối Với Hàng Rào Bảo Vệ Da
Lợi Khuẩn Và Vai Trò Đối Với Hàng Rào Bảo Vệ Da
 Cường Giáp Nên Kiêng Ăn Gì Và Lưu Ý Gì Về Chế Độ Ăn Để Phục Hồi Sức Khỏe?
Cường Giáp Nên Kiêng Ăn Gì Và Lưu Ý Gì Về Chế Độ Ăn Để Phục Hồi Sức Khỏe?
 Suy Dinh Dưỡng Ở Người Trưởng Thành Khắc Phục Như Thế Nào?
Suy Dinh Dưỡng Ở Người Trưởng Thành Khắc Phục Như Thế Nào?
 Căng Thẳng, Stress Ở Phụ Nữ Mang Thai Và Sau Sinh Nguy Hiểm Như Thế Nào?
Căng Thẳng, Stress Ở Phụ Nữ Mang Thai Và Sau Sinh Nguy Hiểm Như Thế Nào?
.png)
건강미인의 에너지 비법
TRUNG TÂM TINH DẦU THÔNG ĐỎ HÀN QUỐC EDALLY BH
 BT 09 - KĐT Resco, Quận Bắc Từ Liêm, Hà Nội, Việt Nam
BT 09 - KĐT Resco, Quận Bắc Từ Liêm, Hà Nội, Việt Nam
.png) Phố Tăng, Đông Hưng, Thái Bình, Việt Nam
Phố Tăng, Đông Hưng, Thái Bình, Việt Nam
 0902.158.663 / 0908.062.668
0902.158.663 / 0908.062.668
.png) edallyhq@gmail.com
edallyhq@gmail.com